Különleges fehérjéket fedeztek fel magyar kémikusok
Az ELTE és a Szegedi Tudományegyetem kutatói az S100 fehérjecsaládot vizsgálva arra az eredményre jutottak, hogy a sokféle betegség kialakulásában szerepet játszó fehérjecsalád körülbelül fele „szabados életet él”, azaz gyakran váltogatja molekuláris partnereit.
Nyitray László, az ELTE Biokémiai Tanszék kutatója és munkatársai évek óta tanulmányozzák az S100 nevű különleges fehérje viselkedését. Legújabb kutatásukban a fehérjecsalád kölcsönhatási hálózatát térképezték fel minden eddiginél pontosabban. A Scientific Reports című folyóiratban megjelent eredményeik hozzájárulnak a tumorok, neurodegeneratív és gyulladásos betegségek kezelésében hatékony és a legkevesebb mellékhatással rendelkező gyógyszerek előállításához – olvasható az ELTE Természettudományi Karának hétfői közleményében.
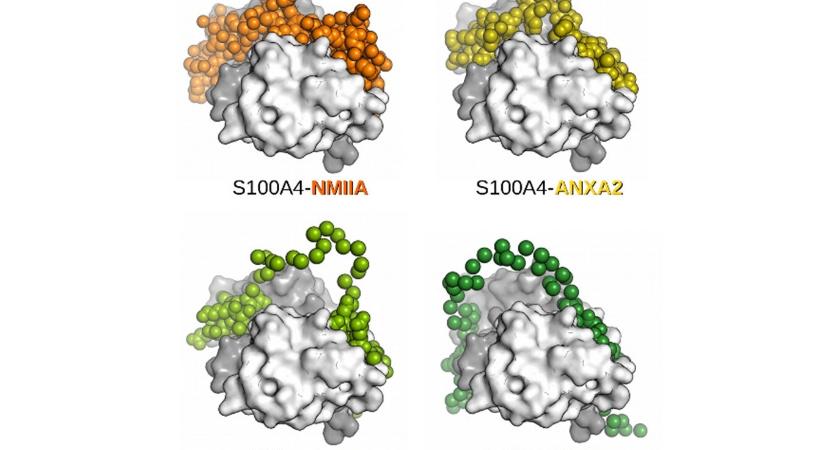
A vizsgálat során a kutatók arra keresték a választ, hogy a promiszkuitás létezik-e a molekulák, a fehérjék világában, vannak-e a molekuláris partnereiket gyakran váltogató fehérjék.
Nyitray László, az ELTE Biokémiai Tanszék professzorának munkacsoportja, együttműködésben Martinek Tamás, a Szegedi Tudományegyetem Orvosi Vegytani Intézetének „Lendület” pályázat nyertes kutatócsoportjával, a fehérje-fehérje kölcsönhatások körében járt utána a promiszkuitásnak.
Magyarázatuk szerint minél több fehérje-fehérje kapcsolat van egy élőlényben, annál komplexebb szerveződésű. Az élő rendszeren belül a fehérje–fehérje kölcsönhatások összessége, az úgynevezett interaktom a molekuláris szintű komplexitás legfontosabb eleme. A fehérjék egymással (és más biomolekulákkal) kialakított fizikai kapcsolata az egyetlen kommunikációs eszköz, amivel a „sejtváros lakói”, a makromolekulák információt tudnak cserélni egymással.
Könyvtárba szedték őket
A Scientific Reports című folyóiratában megjelent közlemény egy korábban megkezdett kutatás folytatása. Ennek során, egy evolúciós értelemben fiatal, csak a gerinces állatokban előforduló, S100 fehérjecsalád 20 tagját kezdték el tanulmányozni.
Ezek a fehérjék, mint írták, a sejtekben kitüntetett szabályozószerepet betöltő kalciumionokat kötik meg, ennek hatására pedig más fehérjékkel képesek kölcsönhatásba lépni, és ezáltal nagyszámú fiziológiás, és sajnos patológiás folyamatban játszanak szerepet. Ez utóbbi mindig az S100 fehérjék túlzott termelődésével függ össze.
A sokféle betegségben, például áttéteket képző tumorok, neurodegeneratív és gyulladásos betegség kialakulásában betöltött szerepük miatt az S100 fehérjecsalád komoly diagnosztikai és terápiás jelentőséggel bír.
A beszámoló szerint a kutatók a most közölt munkában egy hattagú, két aminosav-oldalláncot utánzó foldemerekből álló molekulakönyvtár segítségével az S100 fehérjecsalád összes tagjának a kötőfelszínét le tudták tapogatni.
A foldamerek olyan, a fehérje–fehérje kölcsönhatásokban részt vevő szerkezeti elemeket utánzó, viszonylag kis méretű szintetikus oligomerek, úgynevezett biomimetikumok, melyek a gyógyszerfejlesztés ígéretes eszközei, főleg olyan esetekben, amikor a célfehérjéhez szerves kismolekulával nem lehet fajlagos kötést elérni – írták.
Az összegzés szerint az S100 család körülbelül fele „szabados életet él”, egyértelműen nem válogat a partnerek (foldamerek) között, míg a másik fele csak egy-két partnerrel, vagy eggyel sem létesít fizikai kapcsolatot.
Mint a közleményben kiemelték, az eredményeket az S100 fehérjék patológiás szerepét megszüntetni kívánó gátlószer-fejlesztéseknél feltétlenül figyelembe kell venni, amennyiben hatékony és a legkevesebb mellékhatással rendelkező gyógyszert kívánnak előállítani.
Iratkozz fel speciálisan erre a célra kialakított Telegram-csatornánkra, melyen teljes egészében megosztjuk cikkeinket! A telefonod háttérben futó üzemmódban fogja betölteni az aktuális híreket, így nem fogsz lemaradni a legfontosabb eseményekről!
Feliratkozás