Az Európai Unió hatósága nemet mondott egy új Alzheimer-gyógyszerre
Az Európai Gyógyszerügynökség (EMA) elutasította az Alzheimer-kór elleni egyik új gyógyszerre vonatkozó ajánlást. Az EMA bejelentette, hogy a lecanemab antitest súlyos mellékhatásainak nagyobb a kockázata, mint a várt pozitív hatás.
Tavaly ősszel, az Alzheimer világnapon még két olyan készítményt is reménykeltőként harangoztak be a tudósok, amelyek képesek lelassítani a demenciás betegség hatásait. Az egyiknek a hatóanyagát, a lecanemabot azonban Európában várhatóan nem fogják forgalmazni.
Az EU gyógyszerügynöksége azért utasította el az antitestre vonatkozó ajánlást, mert úgy látta, hogy a súlyos mellékhatásoknak nagyobb a kockázata, mint a várt pozitív hatás.
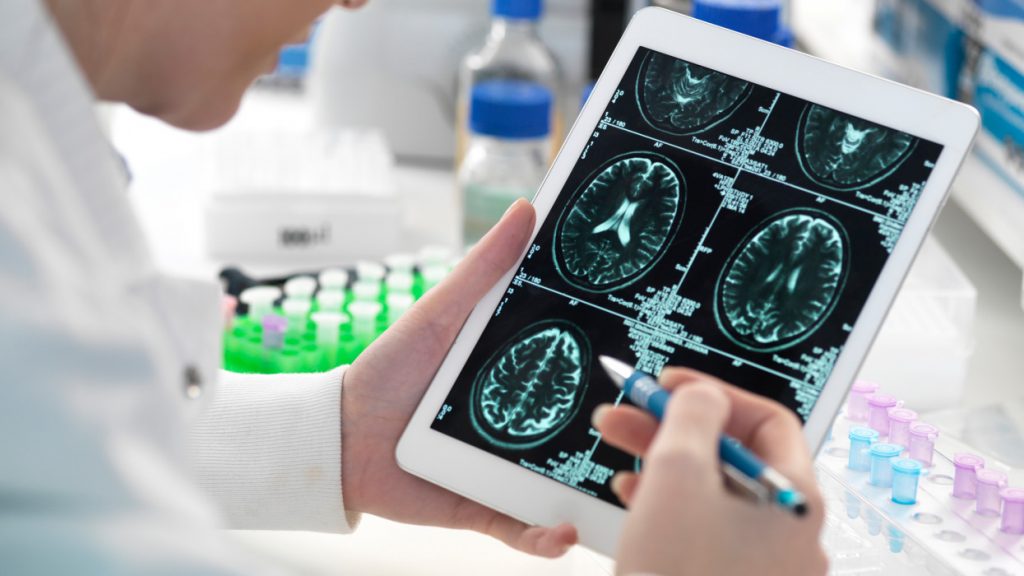
A lecanemab mellékhatásai közül az EMA különösen a mikrovérzést és az agyi ödémát emelte ki. Ezen kockázatok miatt a terápiát rendszeresen ellenőrizni kell MRI-vizsgálatokkal. A hatóság illetékes bizottsága ezért arra az általános következtetésre jutott, hogy „a készítménynek a kognitív hanyatlás lassításában megfigyelt hatása nem ellensúlyozza a súlyos mellékhatások kockázatát”.
A lecanemab – kereskedelmi nevén Leqembi – 2023 eleje óta kapható az USA-ban a korai stádiumú Alzheimer-kór kezelésére. Bár a terápia nem javítja a tüneteket, ebben a stádiumban némileg lassíthatja a betegség előrehaladását. Az antitest ezért csak az Alzheimer-kóros betegek kevesebb mint tíz százalékának kezelésére lenne alkalmas.
A Földön 55 millióan szenvednek ettől a betegségtől.
Az EMA ajánlása, hogy ne engedélyezzék a gyógyszert az európai piacon, vegyes reakciókat váltott ki az Alzheimer-kutatók körében. „Igaz, hogy az engedélyezés pozitív jel lett volna a demenciagyógyszerek fejlesztésének további innovációi számára. Másfelől viszont a lecanemab kognitív előnyei a legjobb esetben is szerények, és jelentős mellékhatásokkal járnak” – mondta Ivan Koychev oxfordi pszichiáter.
Az Európai Unióban az EMA ajánlása szükséges új gyógyszerek engedélyezéséhez. A hatóság szerint az engedélyezési kérelmet benyújtó Eisai cég 15 napon belül kérheti az újbóli vizsgálatot.
Iratkozz fel speciálisan erre a célra kialakított Telegram-csatornánkra, melyen teljes egészében megosztjuk cikkeinket! A telefonod háttérben futó üzemmódban fogja betölteni az aktuális híreket, így nem fogsz lemaradni a legfontosabb eseményekről!
Feliratkozás